Bài 13: Luyện tập: Tính chất của nitơ, photpho và các hợp chất của chúng
200 View


Lý thuyết
Tính chất hóa học của Nitơ và hợp chất của chúng
I. Đơn chất nitơ
- Cấu hình electron nguyên tử: 1s22s22p3, nguyên tử có 3 electron độc thân. Các số oxi hóa: -3, 0, +1, +2, +3, +4, +5. - Phân tử N2 có liên kết ba bền vững nên N2 khá trơ ở điều kiện thường. - Có số oxi hóa trung gian nên N2 thể hiện cả tính khử và tính oxi hóa.II. Hợp chất của nitơ
1. Amoniac - Là chất khí tan rất nhiều trong nước. - Tính bazo yếu: + Phản ứng với nước: NH3 + H2O ⇋ NH4+ + OH-. + Phản ứng với axit tạo muối amoni: NH3 + HCl → NH4Cl (amoni clorua). + Phản ứng với dung dịch muối: AlCl3 + 3NH3 + 3H2O → Al(OH)3↓ + 3NH4Cl Al3+ + 3NH3 + 3H2O → Al(OH)3↓ + 3NH4+ - Tính khử: phản ứng được với oxi, clo và khử một số oxit kim loại. - Khả năng tạo phức chất tan:
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2
AgCl + 2NH3 → [Ag(NH3)2]Cl
2. Muối amoni
- Dễ tan trong nước, là chất điện li mạnh.
- Trong dung dịch, ion NH4+ là axit yếu: NH4+ + H2O ⇋ NH3 + H3O+.
- Tác dụng với dung dịch kiềm:
- Khả năng tạo phức chất tan:
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2
AgCl + 2NH3 → [Ag(NH3)2]Cl
2. Muối amoni
- Dễ tan trong nước, là chất điện li mạnh.
- Trong dung dịch, ion NH4+ là axit yếu: NH4+ + H2O ⇋ NH3 + H3O+.
- Tác dụng với dung dịch kiềm: 3. Axit nitric
- Là axit mạnh.
- Tính axit: HNO3 → H+ + NO3-.
- Tính oxi hóa mạnh: Kim loại hay phi kim khi gặp axit HNO3 đều bị oxi hóa về trạng thái oxi hóa cao nhất.
+ Oxi hóa hầu hết các kim loại (trừ vàng (Au) và platin(Pt)).
Tùy nồng độ axit và tính khử của kim loại sẽ cho sản phẩm khử khác nhau: NO2, NO, N2O, N2, NH4NO3.
Cu + 4HNO3(đ) → Cu(NO3)2 + 2NO2 + 2H2O.
3Cu + 8HNO3(l) → 3Cu(NO3)2 + 2NO + 4H2O.
+ Oxi hóa được nhiều phi kim và các hợp chất có tính khử.
S + 6HNO3(đ) → H2SO4 + 6NO2 + 2H2O
3FeO + 10HNO3(d) → 3Fe(NO3)3 + NO + 5H2O
3H2S + 2HNO3(d) → 3S + 2NO + 4H2O
4. Muối nitrat
- Dễ tan trong nước, là chất điện li mạnh.
- Dễ bị nhiệt phân hủy:
2KNO3 → 2KNO2 + O2
2Cu(NO3)2 → 2CuO + 4NO2 + O2
2AgNO3 → 2Ag + 2NO2 + O2
- Nhận biết ion NO3-:
Sử dụng hỗn hợp vụn đồng và dung dịch H2SO4 loãng, đun nóng:
3Cu + 8H+ + 2NO3- → 3Cu2+ (dd màu xanh) + 2NO↑ + 4H2O
2NO + O2 (không khí) → 2NO2 (màu nâu đỏ)
3. Axit nitric
- Là axit mạnh.
- Tính axit: HNO3 → H+ + NO3-.
- Tính oxi hóa mạnh: Kim loại hay phi kim khi gặp axit HNO3 đều bị oxi hóa về trạng thái oxi hóa cao nhất.
+ Oxi hóa hầu hết các kim loại (trừ vàng (Au) và platin(Pt)).
Tùy nồng độ axit và tính khử của kim loại sẽ cho sản phẩm khử khác nhau: NO2, NO, N2O, N2, NH4NO3.
Cu + 4HNO3(đ) → Cu(NO3)2 + 2NO2 + 2H2O.
3Cu + 8HNO3(l) → 3Cu(NO3)2 + 2NO + 4H2O.
+ Oxi hóa được nhiều phi kim và các hợp chất có tính khử.
S + 6HNO3(đ) → H2SO4 + 6NO2 + 2H2O
3FeO + 10HNO3(d) → 3Fe(NO3)3 + NO + 5H2O
3H2S + 2HNO3(d) → 3S + 2NO + 4H2O
4. Muối nitrat
- Dễ tan trong nước, là chất điện li mạnh.
- Dễ bị nhiệt phân hủy:
2KNO3 → 2KNO2 + O2
2Cu(NO3)2 → 2CuO + 4NO2 + O2
2AgNO3 → 2Ag + 2NO2 + O2
- Nhận biết ion NO3-:
Sử dụng hỗn hợp vụn đồng và dung dịch H2SO4 loãng, đun nóng:
3Cu + 8H+ + 2NO3- → 3Cu2+ (dd màu xanh) + 2NO↑ + 4H2O
2NO + O2 (không khí) → 2NO2 (màu nâu đỏ)
Tính chất hóa học của Photpho và hợp chất của chúng
I. Đơn chất của photpho
 Vì P có các số oxi hoá: -3, 0, +3, +5 nên P có thể thể hiện tính khử và tính oxi hoá.
a. Tính oxi hoá: P0 → P-3
Tác dụng với một số kim loại hoạt động, tạo ra photphua kim loại.
Ví dụ:
Vì P có các số oxi hoá: -3, 0, +3, +5 nên P có thể thể hiện tính khử và tính oxi hoá.
a. Tính oxi hoá: P0 → P-3
Tác dụng với một số kim loại hoạt động, tạo ra photphua kim loại.
Ví dụ:  b. Tính khử: P0 → P+3, P0 → P+5
- Tác dụng với oxi: Khi đốt nóng, photpho cháy trong không khí tạo ra các oxit của photpho:
b. Tính khử: P0 → P+3, P0 → P+5
- Tác dụng với oxi: Khi đốt nóng, photpho cháy trong không khí tạo ra các oxit của photpho:
 - Tác dụng với clo: Khi cho clo đi qua P nóng chảy, sẽ thu được các hợp chất photpho clorua:
- Tác dụng với clo: Khi cho clo đi qua P nóng chảy, sẽ thu được các hợp chất photpho clorua:
 - Tác dụng với hợp chất:
6P + 5KClO3 → 3P2O5 + 5KCl
- Tác dụng với hợp chất:
6P + 5KClO3 → 3P2O5 + 5KCl
II. Axit photphoric
- Là axit 3 nấc, có độ mạnh trung bình. - Không có tính oxi hóa. - Tạo ra 3 loại muối khi tác dụng với dung dịch kiềm do dung dịch nó phân li ra 3 nấc: H3PO4 ⇋ H+ + H2PO4- ⇒ k1 = 7, 6.10-3 H2PO4- ⇋ H+ + HPO42- ⇒ k2 = 6,2.10-8 HPO42- ⇋ H+ + PO43- ⇒ k3 = 4,4.10-13 ⇒ nấc 1 > nấc 2 > nấc 3. Ví dụ: H3PO4 + NaOH → NaH2PO4 + H2O H3PO4 + 2NaOH → Na2HPO4 + 2H2O H3PO4 + 3NaOH → Na3PO4 + 3H2OIII. Muối photphat
1. Phân loại Axít photphoric tạo ra 3 loại muối: - Muối photphat trung hòa: Na3PO4, Ca3(PO4)2, … - Muối đihidrophotphat: NaH2PO4, Ca(H2PO4)2, … - Muối hidrophotphat: Na2HPO4, CaHPO4, … 2. Tính tan - Muối dễ tan trong nước: + Tất cả các muối photphat của Na, K, NH4+. + Muối dihidrophotphat của các kim loại khác. - Muối không tan hoặc ít tan trong nước: + Muối hidrophotphat và muối photphat trung hòa của các kim loại trừ của Na, K, NH4+. 3. Nhận biết ion photphat Thuốc thử là bạc nitrat. 3Ag+ + PO43- → Ag3PO4↓ (màu vàng)Bài 1 (trang 61 SGK Hóa 11):
Hãy cho biết số oxi hóa của N và P trong các phân tử và ion sau đây NH3, NH4+, NO2-, NO3-, NH4HCO3 , P2O3, PBr5, PO43–, KH2PO4, Zn3(PO4)2. Lời giải:
Bài 2 (trang 61 SGK Hóa 11):
Trong các công thức sau đây, chọn công thức hóa học đúng của magie photphua: A. Mg3(PO4)2 B. Mg(PO3)2 C. Mg3P2 D. Mg2P2O7 Lời giải: Đáp án CBài 3 (trang 61 SGK Hóa 11):
a) Lập các phương trình hóa học sau đây: NH3 + Cl2 (dư) → N2 + .. NH3(dư) + Cl2 → NH4Cl + …. NH3 + CH3COOH → … (NH4)3PO4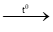 H3PO4 + …
Zn(NO3)2
H3PO4 + …
Zn(NO3)2 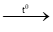 …
b) Lập các phương trình hóa học ở dạng phân tử và dạng ion rút gọn của phản ứng giữa các chất sau đây trong dung dịch:
(1) K3PO4 và Ba(NO3)2
(2) Na3PO4 và CaCl2
(3) Ca(H2PO4)2 và Ca(OH)2 với tỉ lệ mol 1:1
(4) (NH4)3PO4 + Ba(OH)2
Lời giải:
a)
…
b) Lập các phương trình hóa học ở dạng phân tử và dạng ion rút gọn của phản ứng giữa các chất sau đây trong dung dịch:
(1) K3PO4 và Ba(NO3)2
(2) Na3PO4 và CaCl2
(3) Ca(H2PO4)2 và Ca(OH)2 với tỉ lệ mol 1:1
(4) (NH4)3PO4 + Ba(OH)2
Lời giải:
a)
 b)
(1) 2K3PO4 + 3Ba(NO3)2 → Ba3(PO4)2 ↓ + 6KNO3
Ba2+ + 2PO43- → Ba3(PO4)2 ↓
(2) 2Na3PO4 + 3CaCl2 → Ca3(PO4)2 ↓ + 6NaCl
Ca2+ + 2PO43- → Ca3(PO4)2 ↓
(3) Ca(H2PO4)2 + Ca(OH)2 → 2CaHPO4 + 2H2O
H2PO4- + OH- → HPO42- + H2O
(4) 2(NH4)3PO4 + 3Ba(OH)2 → Ba3(PO4)2 ↓ + 6NH3 ↑ + 6H2O
6NH4+ + 2PO43- + 3Ba2+ + 6OH- → Ba3(PO4)2 ↓ + 6NH3 ↑ + 6H2O
b)
(1) 2K3PO4 + 3Ba(NO3)2 → Ba3(PO4)2 ↓ + 6KNO3
Ba2+ + 2PO43- → Ba3(PO4)2 ↓
(2) 2Na3PO4 + 3CaCl2 → Ca3(PO4)2 ↓ + 6NaCl
Ca2+ + 2PO43- → Ca3(PO4)2 ↓
(3) Ca(H2PO4)2 + Ca(OH)2 → 2CaHPO4 + 2H2O
H2PO4- + OH- → HPO42- + H2O
(4) 2(NH4)3PO4 + 3Ba(OH)2 → Ba3(PO4)2 ↓ + 6NH3 ↑ + 6H2O
6NH4+ + 2PO43- + 3Ba2+ + 6OH- → Ba3(PO4)2 ↓ + 6NH3 ↑ + 6H2O
Bài 4 (trang 61 SGK Hóa 11):
Từ hiđro, clo, nitơ và các hóa chất cần thiết, hãy viết các phương trình hóa học (có ghi rõ điều kiện phản ứng) điều chế phân đạm amoni clorua. Lời giải:
Bài 5 (trang 62 SGK Hóa 11):
Viết phương trình hóa học thực hiện các dãy chuyển hóa sau: Lời giải:
Lời giải:

 Bài 6 (trang 62 SGK Hóa 11): Hãy đưa ra những phản ứng đã học có sự tham gia của đơn chất photpho, trong đó số oxi hóa của photpho:
a. Tăng
b. Giảm
Lời giải:
Bài 6 (trang 62 SGK Hóa 11): Hãy đưa ra những phản ứng đã học có sự tham gia của đơn chất photpho, trong đó số oxi hóa của photpho:
a. Tăng
b. Giảm
Lời giải:

Bài 7 (trang 62 SGK Hóa 11):
Khi cho 3,00 g hỗn hợp Cu và Al tác dụng với dung dịch HNO3 đặc dư, đun nóng, sinh ra 4,48 lít khí duy nhất NO2 (đktc). Xác định phần trăm khối lượng của mỗi kim loại trong hỗn hợp? Lời giải: Gọi nAl = x (mol), nCu = y (mol); nNO2 = Theo pt: nNO2(1) = 3. nAl = 3.x mol
nNO2(2) = 2. nCu = 2y mol
⇒ Tổng nNO2 = 3x + 2y = 0,2 mol
Ta có hệ phương trình
Theo pt: nNO2(1) = 3. nAl = 3.x mol
nNO2(2) = 2. nCu = 2y mol
⇒ Tổng nNO2 = 3x + 2y = 0,2 mol
Ta có hệ phương trình


Bài 8 (trang 62 SGK Hóa 11)
: Cho 6,00 g P2O5 vào 25,0 ml dung dịch H3PO4 6,00% (D = 1,03 g/ml). Tính nồng độ phần trăm H3PO4 trong dung dịch tạo thành? Lời giải: mdd H3PO4 = V. D = 25. 1,03 = 25,75g mH3PO4(sau phản ứng) = 1,545 + 8,282 = 9,827(g)
Khối lượng dung dịch sau phản ứng = 25,75 + 6 = 31,75(g)
mH3PO4(sau phản ứng) = 1,545 + 8,282 = 9,827(g)
Khối lượng dung dịch sau phản ứng = 25,75 + 6 = 31,75(g)
Bài 9 (trang 62 SGK Hóa 11):
Cần bón bao nhiêu kg phân đạm amoni nitrat chứa 97,5% NH4NO3 cho 10,0 hecta khoai tây, biết rằng 1,00 hecta khoai tây cần 60,0 kg nitơ? Lời giải: 10ha khoai tây cần 60. 10 = 600 kg nitơ Bảo toàn nguyên tố Nito: ⇒ 1 mol (80g) NH4NO3 tạo thành 1 mol (28g)N2 Lượng NH4NO3 cần để có 600kg N2 là
Bài tập trắc nghiệm
Bài 1: Để phân biệt các mẫu phân bón sau : (NH4)2SO4, NH4Cl và Ca(H2PO4)2 cần dùng thuốc thử là A. dung dịch BaCl2. B. dung dịch Ba(OH)2. C. dung dịch HCl. D. dung dịch NaOH.
Đáp án: B
Đáp án: A
Đáp án: D
Đáp án: A
nNH3 = 2n(NH4)2SO4 = 0,02 mol
nH3PO4 = 0,04 mol
nNH3 : nH3PO4 = 1 : 2 ⇒ tạo muối NH4H2PO4
Đáp án: C
Đáp án: D
nNO = x mol; nN2O = y mol;
⇒ 30x + 44y = 5,75 g (1)
Bảo toàn e ta có: ne cho = ne nhận = 2nH2 = 0,8mol
⇒ 3x + 8y = 0,8 (2)
Từ (1)(2) ⇒ x = 0,1 mol; y = 0,0625 mol ⇒ VY = 3,64 lít
Đáp án: D
2Cu(NO3)2 -H = 80%→ 2CuO + 4NO2 (4x) + O2 (x mol)
mc/rắn giảm = mkhí = 6,58 – 4,96 = 1,62 gam ⇒ mNO2 + mO2 = 1,62
46. 4x + 32x = 1,62 ⇒ x = 0,0075 mol
nNO2 = nHNO3 = nH+ = 0,03 ⇒ [H+] = 0,1 ⇒ pH = 1,0
Đáp án: A
nCa3(PO4)2 = 0,235 kmol; nCaCO3 = 0,26Kmol
Điều chế supephotphat đơn: nH2SO4 = 2 nCa3(PO4)2 + nCaCO3 = 0,73 kmol
⇒ mdd = 0,73. 98 : 65% = 110,2 kg
Đáp án: A
Bảo toàn nguyên tố:
nP2O5 = 1/2. nNa2HPO4 + 1/2. nNaH2PO4 = 0,2 mol = a
nNaOH = 2nNa2HPO4 + nNaH2PO4 = 0,55 mol ⇒ CM NaOH = 2,75 mol
Đáp án: C
PX3 (x) + 3H2O → 3HX (3x) + H3PO3 (x mol)
nNaOH = nHX + 2nH3PO3 = 5x = 0,09 mol (axit H3PO3 là axit 2 nấc )
⇒ x = 0,018 mol
⇒ PX3 = 4,878 : 0,018 = 271 ⇒ X = 80 (Br)
Đáp án: A
Đáp án: A
Đáp án: D
Đáp án: B
Đáp án: C
Đáp án: A
Các bài viết liên quan
Các bài viết được xem nhiều nhất
5 tác phẩm trọng tâm ôn thi THPT Quốc gia 2024 môn Ngữ Văn khả năng...
26321 View
Đáp án CHÍNH THỨC đề thi tốt nghiệp THPT 2023 từ Bộ GD&ĐT (Tất cả...
1212 View
Đề thi tốt nghiệp THPT Quốc gia năm 2023 môn Giáo dục công dân và gợi...
1152 View
Đề thi tốt nghiệp THPT Quốc gia năm 2023 môn Địa lí và gợi ý giải...
1141 View
Link tra cứu điểm thi THPT Quốc gia 2023 toàn quốc 63 tỉnh thành. Cách xem...
1053 View
Theo dõi Captoc trên




